|
|
Acer 30-32. 08038 BARCELONA |
Departamento
Comercial: |
gestioncomercial@cromlab.es administracion@cromlab.es laboratorio@cromlab.es |
|
 |
|
|
|
|
Reactivos de Derivatización PIERCE |
|
   |
|
DERIVATIZACIÓN EN GC |
La literatura química
contiene muchos datos sobre derivatización, muchos de los cuales se
refieren a compuestos particulares, a clases de compuestos ya reactivos
químicos. Se reconocen como estándares en el campo de la derivatización
analítica a dos libros:
Se derivatizan compuestos o mezclas de compuestos antes del análisis por los siguientes motivos:
|
||||||
| 1. Idoneidad | ||||||
| A menudo los compuestos no pueden analizar porque no están en una forma adecuada para una técnica analítica particular. Los ejemplos incluyen compuestos no volátiles para análisis por GC(8,9,10), compuestos insolubles en análisis por HPLC y materiales no estables en las condiciones analíticas(11), El procedimiento de derivatización modifica la estructura química de los compuestos permitiendo el análisis por la técnica deseada(12). | ||||||
| 2. Eficacia | ||||||
| El análisis directo puede resultar difícil si los compuestos interaccionan entre sí o con la columna. Estas interacciones puede causar una resolución pobre y/o picos asimétricos que causan una integración y cuantificación difícil o poco práctica. Esta interferencia puede reducirse con la conversión a productos derivados(13,14). Los compuestos que coeluyen puede separarse muchas veces usando los métodos de derivatización adecuados. | ||||||
| 3. Detectabilidad | ||||||
|
Al aumentar la necesidad
de detectar compuestos en cantidades cada vez más pequeñas, resulta
importante ampliar el rango de detección de los productos en cuestión.
Esta mayor sensibilidad puede conseguirse mediante el uso de un detector
específico frente a átomos o grupos funcionales específicos. Otra aproximación popular hacia el aumento de la detectabilidad consiste en la derivatización. Una sensibilidad mayor se puede conseguir aumentando la cantidad de compuesto a analizar o vía la introducción de átomos o grupos funcionales que interacciones fuertemente con el detector(16,17). Esta técnica se usa en aplicaciones gascromatográficas, mediante la introducción de halógenos para detectores de captura de electrones(18,19), o produciendo TMS derivados para producir fragmentaciones de iones fácilmente identificables en MS(20). |
||||||
| Tipos de Derivados | ||||||
|
Los compuestos que
contienen grupos funcionales con hidrógenos activos (-COOH, -OH, -NH y -SH)
se suelen derivatizar antes de su análisis por cromatografía de gases.
Estos grupos funcionales tienden a formar enlaces de hidrógeno
intermolecular que afectan a la volatilidad, pueden interactuar
negativamente con la fase estacionaria de la columna y pueden ser
térmicamente inestables. La sililación, acilación y la alquilación son
las técnicas de derivatización usadas para alterar estos grupos
funcionales mejorando sus características térmicas y cromatográficas. El procedimiento ideal de derivatización deberá:
|
||||||
| Reacciones: Sililación | ||||||
|
Los derivados con silicio son los más
ampliamente usados en aplicaciones de cromatografía de gases. En general
se forman por substitución de los hidrógenos activos de ácidos,
alcoholes, tioles, aminas, amidas y cetonas y aldehídos enolizables con
grupos TMS (TriMetilSilil). Existe una amplia gama de reactivos
disponibles para la introducción de estos grupos, que difieren en su
reactividad, selectividad y reacciones secundarias y en el carácter de
los productos de reacción. Existe una amplia literatura disponible que
permite seleccionar el reactivo de sililación más adecuado para cada
problema analítico particular (1,2). Los reactivos de sililación y los derivados TMS son inestables hidrolíticamente y deben ser protegidos frente a la humedad. Sin embargo el grado de hidrólisis de cada reactivo y derivado es diferente, y, en algunos casos, es posible preparar derivados en presencia de pequeñas cantidades de humedad(21), o aislar y purificar derivados por extracción en un solvente orgánico y lavado con soluciones acuosas(22). Los reactivos que introducen un grupo t-Butilsililo en lugar de un grupo TMS se desarrollaron para presentar una estabilidad hidrolítica mayor(23). Estos derivados ofrecen una mayor estabilidad frente a la hidrólisis y generan perfiles de fragmentación específicos, lo que los hacen muy útiles en aplicaciones de GCMS(24). La mayoría de los derivados TMS o TBDS tienen una excelente estabilidad térmica y resultan adecuados para una amplia gama de condiciones de inyector y columna. Sin embargo, puesto que los reactivos de sililación modificarán prácticamente todos los hidrógenos activos, es importante que no se inyecten en columnas con fases estacionarias que contengan dichos grupos funcionales. Ejemplos de fases no compatibles son los polietilénglicoles (TR-WAX o TR-WaxMS) y fases para ácidos libres (TR-FFAP). |
||||||
| Reacciones: Acilación | ||||||
|
La acilación es la conversión de
compuestos que contengan hidrógenos activos como -H, -SH y -NH en
ésteres. tioésteres y amidas mediante la acción de una ácido carboxílico
o un derivado de un ácido carboxílico(25). En aplicaciones
cromatográficas, la reacción de acilación se usa principalmente para
convertir las clases anteriores de compuestos en derivados que sean más
adecuados para cromatografía(26) o que dan una mayor
respuesta en la detección cromatográfica que el compuesto original(27). Un ejemplo importante de esta aplicación es la inserción de grupos perfluoroacetilo en una molécula para incrementar la respuesta en detectores de Captura de Electrones (ECD). Los acilderivados resultan también útiles en aplicaciones de Espectrometría de Masas en las que modifican los perfiles de fragmentación de los compuestos a estudiar(28). |
||||||
| Reacciones: Alquilación | ||||||
|
La alquilación es la substitución de un
hidrógeno activo por un grupo alifático o alifático-aromático (bencilo)(29).Esta
técnica se usa para modificar los compuestos con hidrógenos activos como
ácidos carboxílicos y fenoles. La aplicación principal de esta técnica
es la conversión de ácidos orgánicos en ésteres, que permiten mejores
cromatogramas que los ácidos libres. Además la reacciones de alquilación pueden usarse para preparar éteres, tioéteres y tioésteres, N-alquilaminas y amidas(30). A medida que disminuye la acidez de los hidrógenos activos, ha de aumentarse la fuerza del agente alquilante. Al ser las condiciones más extremas y los reactivos más potentes, la selectividad y aplicabilidad de los métodos resulta más limitada. |
||||||
| DERIVATIZACIÓN EN HPLC | ||||||
 La
falta de un detector universal en HPLC que ofrezca una alta sensibilidad
(además de cierto grado de selectividad) ha obligado al desarrollo de
algunos procedimientos de derivatización adecuados. La derivatización es
la modificación química de un compuesto para obtener otro con
propiedades más adecuadas para el procedimiento analítico utilizado.
Resulta una herramienta analítica que puede usarse para ofrecer
selectividad y sensibilidad. La
falta de un detector universal en HPLC que ofrezca una alta sensibilidad
(además de cierto grado de selectividad) ha obligado al desarrollo de
algunos procedimientos de derivatización adecuados. La derivatización es
la modificación química de un compuesto para obtener otro con
propiedades más adecuadas para el procedimiento analítico utilizado.
Resulta una herramienta analítica que puede usarse para ofrecer
selectividad y sensibilidad.Para desarrollar un protocolo de derivatización existen varios requerimientos:
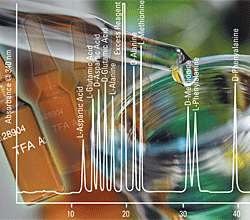
En derivatización para
HPLC pueden usarse técnicas de pre y de post derivatización, además de
reacciones off y on-line. Las técnicas pre-columna ofrecen una mayor
simplicidad técnica y se pueden usar para mejorar la estabilidad, la
resolución, la simetría de pico y aumentar o disminuir el tiempo de
retención de los solutos. FDAA (Reactivo de Marley), permite la
separación y cuantificación de los isómeros ópticos de los aminoácidos
(ver cromatograma). Las técnicas post-columna se utilizan principalmente
para mejorar la selectividad y la sensibilidad. |
||||||
| Literatura | ||||||
 |
El "Handbook of
Analytical Derivatization Reactions", por Daniel R. Knapp,
es una colección general de métodos de derivatización general
para Cromatografía y Espectrometría de Masas, para la formación
de derivados covalentes antes del análisis. Los métodos presentados en este volumen están organizados según el tipo de muestra a derivatizar. Los métodos incluyen fórmulas estructurales, guías experimentales y comentarios útiles. El índice está estructurado de tal manera que se pueda encontrar rápidamente el método de interés listo para su aplicación. |
|||||
|
||||||
 |
Reactivos, Solventes y Accesorios Thermo Scientific Pierce | |||||
|
||||||
| Referencias | ||||||
|
||||||
Copyright© 2006-2014 CromLab S.L. Prohibida la reproducción total o parcial sin consentimiento escrito del propietario.